11月2日,Journal of Medical Virology杂志在线发表题为“SARS-CoV-2 ORF7a blocked autophagy flux by intervening in the fusion between autophagosome and lysosome to promote viral infection and pathogenesis” 的研究论文,揭示了SARS-CoV-2 ORF7a通过干预自噬体和溶酶体之间的融合来阻断自噬流,从而促进病毒感染和致病的分子机制,太阳集团tcy8722李顺博士为该论文的第一作者。Journal of Medical Virology为国际知名病毒学SCI期刊,2023年最新影响因子12.7(JCR分区病毒领域排名第2)。南方医科大学、西北工业大学、空军军医大学、加拿大卡尔加里大学共同参与了该研究的合作。相关工作得到了国家自然科学基金、太阳成集团学科创新团队项目等基金的经费支持。

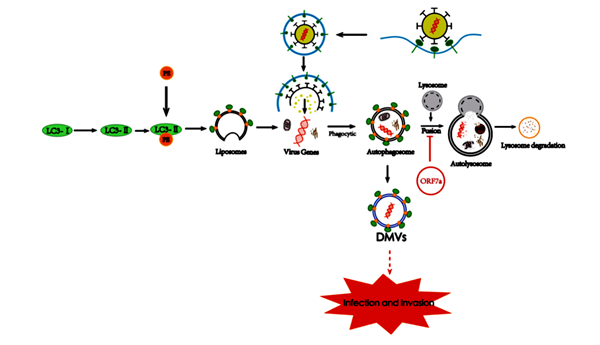
新冠对全球公共卫生构成重大威胁。尽管许多研究已经阐明了SARS-CoV-2的感染过程,但病毒入侵和免疫逃避的潜在机制仍不清楚。全面了解ORF7a的功能可能有助于开发COVID-19的新疗法和临床药物。本研究重点关注 SARS-CoV-2 ORF7a(开放阅读框-7a),它是感染和发病机制中必不可少的开放阅读框(ORF)之一。首先通过分析其理化特性和对ORF7a跨膜域三维晶体结构模型进行预测,发现SARS-CoV-2 ORF7a定位于内质网,通过与 p62 相互作用参与自噬-溶酶体途径。此外,该研究阐明了ORF7a拦截自噬流、促进双膜囊泡形成、逃避宿主自噬-溶酶体降解和抗病毒先天免疫的潜在分子机制。这项研究表明了 ORF7a 可能是一个治疗靶点,而Glecaprevir可能是通过靶向 ORF7a 来对抗 SARS-CoV-2 的潜在药物。
论文第一作者李顺博士现为太阳集团tcy8722免疫学教研室特聘教授,系四川省“天府峨眉计划”青年人才入选者,主要从事细胞自噬与疾病的发生发展关系以及细胞信号转导的分子生物学机制研究。目前主持国家级、省部级项目6项,在国际知名学术期刊Nature Communications、Autophagy等发表SCI论文20余篇。
(太阳集团tcy8722 张先琴)